
加速康复外科:关于头颈部癌症患者游离皮瓣重建术后围手术期疼痛等级和阿片类药物使用的叙述性综述
引言
理论基础/背景
加速康复外科(ERAS)理念以循证医学证据为基础,旨在尽量减少术后发病率和并发症,同时优化术后治疗效果[1]。这种结构化的治疗路径包含了对患者进行术前、术中和术后护理的完整方法,从而促进患者功能的有效恢复[2]。想要实现这一目标,需要系统地践行诊疗步骤,如术前宣教、术前营养支持、保守输血、多模式麻醉(MMA)、术后早期下床活动和营养补充等[3,4]。ERAS指南最早的应用是在结直肠手术中。自2017年Dort等人发布头颈部癌症(HNC)专项指南[3]以来,多项研究探讨了在机构层面实施ERAS指南的可行性及其对HNC患者临床结果的影响[5-9]。
头颈部恶性肿瘤患者的微血管游离皮瓣重建手术操作复杂、牵涉部位广泛且费用昂贵[10]。尽管重建技术不断进步,但鉴于头颈部复杂的解剖结构和精细的行为功能,患者在肿瘤切除术后经常会经历明显的疼痛,并发症发病率也很高[11-13]。这类手术适合不同的临床路径,从而减少患者的合并症、营养不良、疲劳及和长期不能下床活动等影响。基于以上情况,ERAS指南提供了新方法,从而帮助降低接受游离皮瓣重建的HNC患者在围手术期的意外状况发生率[14]。
目前的研究表明,实施ERAS理念可以减少HNC患者在接受肿瘤切除及重建手术后的住院时间(length of stay,LOS)、伤口并发症和再入院率,同时不延长患者在重症监护室的住院时间、提高死亡率或增加二次手术的需求[9]。相对来说,很少有研究探讨ERAS临床路径下的术后疼痛和阿片类药物使用情况。虽然有一些研究报告了ERAS患者人群中术后阿片类药物消耗量的减少和围手术期整体疼痛等级的降低,但目前没有足够的研究数据可以为HNC治疗指南的颁布提供支持[3]。ERAS协会将结直肠手术的临床结果用于指导HNC手术建议,也在侧面反映了相关文献上的空白[3]。
目的
本叙述性综述将评估ERAS治疗方案对接受微血管游离皮瓣组织转移重建手术的HNC患者围手术期疼痛和阿片类药物使用的影响。我们根据叙述性综述报告清单介绍以下内容(可在https://joma.amegroups.com/article/view/5707/rc获取)。
方法
纳入标准
纳入标准为有关遵循ERAS路径的接受游离组织移植重建手术的HNC患者围手术期疼痛和阿片类药物使用情况的主要研究。没有报告ERAS的MMA部分、只包括局部和(或)转瓣术、报告了因放射性骨坏死或其他非恶性病因而接受游离皮瓣重建的患者或未完全接受ERAS路径的研究被排除在外。会议摘要、社论和评论也被排除。
检索方法
在PubMed中检索与ERAS协会发布的HNC指南相关的文献,检索时间为2017年3月1日至2021年11月1日。检索的关键词为“头颈部手术”和“头颈部癌症”以及“围手术期结果”和“疼痛结果”。我们还对主要文献的参考文献列表进行了手动搜索。不限制文献语言、国家或样本量。初步检索结果有30项研究。图1为选择研究的流程图。表1为检索方法总结。

Full table
数据收集
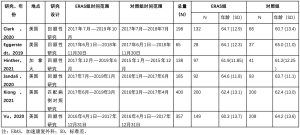
两位独立的研究人员(CXC和RU)对所选摘要进行了初步的标题筛选和审查。7项研究符合纳入标准,但有1篇文章缺乏对照组,经小组讨论后从选定的研究名单中删除。搜索其余6篇研究(见表2)的主要参考文献,提取数据,并填入统一的数据收集表。
Full table
头颈部ERAS理念的构成
不同的医疗机构之间的ERAS理念可能略有不同,但ERAS成功改善了目前最佳的临床实践路径。在本综述中,独立研究人员纳入了多项研究,这些研究明确表明患者接受治疗时严格遵循了HNC相关的ERAS指南。需要对基于证据的核心建议进行细分,特别重要的是围手术期节用阿片类药物的多模式镇痛方案的应用。ERAS方案的其他组成部分包括术前口头或书面宣教、营养优化、目标导向液体管理、术后常规ICU管理、频繁的皮瓣监测和术后早期下床活动。虽然强烈建议采用标准的麻醉方案,但支持这一条件的证据水平较低,不足以排除任何研究。
主要结果
本次叙述性综述的主要结果是遵照ERAS路径接受微血管游离皮瓣组织移植重建的HNC患者的术后疼痛等级和阿片类药物使用情况。
讨论
越来越多的证据表明,遵循ERAS路径的手术患者的临床结果得到了改善[15-17]。对于复合肿瘤切除和游离组织移植重建的患者来说,最近的文献进一步强调了多学科联合在围术期事件及功能恢复方面的优化作用[18]。本综述纳入的研究报告称,在ERAS路径中采用MMA时,疼痛控制会得到改善,阿片类药物的消耗量会降低。这些研究结果支持了以前的相关文献结论,那些文献表明ERAS方案不会对患者的手术体验产生不利影响,反而降低了患者感知到的疼痛和疲劳程度[19]。
多模式镇痛和术后疼痛
一些HNC患者报告的术后疼痛程度最为严重[20]。有效的疼痛管理与患者预后密切相关。疼痛管理不善会导致患者不能活动和机体功能下降,同时间接导致伤口感染、伤口愈合不良、住院时间延长和生活质量下降[21]。疼痛管理不理想可能导致患者在手术后对辅助性肿瘤治疗的医嘱依从性变差,从而使患者的预后恶化。许多研究报告称,HNC患者的疼痛治疗方案严重依赖阿片类药物,目前的疼痛管理是不充分的[22,23]。因此,MMA方案必不可少[8]。
MMA是HNC相关的ERAS理念的一个重要组成部分,目的是改善疼痛控制。精心挑选药物方案后将其实施,以协同实现麻醉状态:无记忆、无体动、抗伤害性感受。常用的药物包括加巴喷丁、非甾体抗炎药、N-甲基-D-天冬氨酸类谷氨酸受体拮抗剂、利多卡因和区域麻醉阻滞剂[24]。历史上,含阿片类药物方案构成了游离皮瓣重建手术后疼痛治疗的基础[25]。因此,未使用过阿片类药物的患者在术后持续使用阿片类药物的概率可高达52%,术前使用过阿片类药物的患者在术后中持续使用阿片类药物的概率可高达82%[26]。因此,MMA是阿片类药物节用策略疼痛管理中的一个重要方法,目的是降低长期滥用阿片类药物的可能性,防止阿片类药物相关死亡的发生[27,28]。此外,HNC患者可能更容易出现阿片类药物滥用。正如Brummett等人所发现的,术前烟草、酒精和药物滥用都与术后长期使用阿片类药物的概率提高有关[29]。HNC患者有酒瘾和烟瘾的概率往往很高,更容易在术后长期使用阿片类药物[22]。
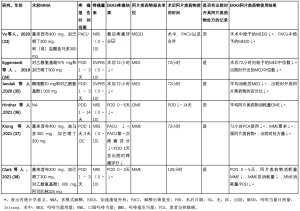
所有研究均使用有11个刻度的数字量表对术后疼痛进行评分。数字评定量表(numeric rating scale,NRS)使用0~10这11个数字来评定疼痛的程度,10表示最痛[30,31]。国防部和退伍军人疼痛评定量表(Defense and Veterans Pain and Rating Scale,DVPRS)在简单的数字量表的基础上,加入了功能词描述、颜色编码和面部表情图片,以改善治疗过渡期的记录[32]。由于这两个量表的操作类似,都是基于数字(0~10),研究小组认为它们具有可比性。所有研究的MMA方案中都使用加巴喷丁。2项研究联合使用了对乙酰氨基酚和加巴喷丁,2项研究使用了曲马多、加巴喷丁和塞来昔布方案。表3呈现了围手术期结果的概况。
Full table
Vu等人首次研究了肿瘤切除和游离皮瓣重建手术前的单剂量MMA与手术中和麻醉后恢复室(PACU)中阿片类药物使用的关系[33]。MMA方案对患者在PACU的最后一次疼痛评分影响较小(Cohen w=0.12;95% CI:0.06~0.24)。Cohen w值小于0.2表示影响小,因此该研究中MMA和非MMA组的平均疼痛评分之间的差异可以忽略不计。与对照组相比,术前至少接受一种MMA药物治疗的患者在PACU中停留的时间更短(平均22 min),平均差异为-0.36(95%CI:-0.63~-0.09)[33]。作者认为,他们的MMA方案立竿见影,在术前用药一次就能减少阿片类药物的需求[33]。单剂量MMA后未观察到疼痛评分的显著下降,这与Du等人报告MMA不改变患者术后疼痛评分的结果一致[27]。
然而,Eggerstedt等人发现,联合使用塞来昔布和加巴喷丁时,患者术后疼痛评分较低[34]。MMA组报告在头颈部游离皮瓣重建后的72小时内,平均疼痛评分(SD)为2.05(1.41),对照组为3.66(1.99)(P=0.001)[34]。这些结果后来被Jandali等人和Hinther等人转载,表3中已列出[35,36]。
Kiong等人的研究表明,与对照组相比,ERAS组的PACU停留时间更短(117±51 min vs141±51 min;P<0.001),且患者在PACU的第一次疼痛评分明显降低(2.5±3.2vs 3.5±3.4;P=0.003)[37]。POD 1天(P=0.892)、POD 3天(P=0.236)和出院日(P=0.273)的平均疼痛评分在ERAS组和对照组之间没有差异,但从POD 1天到出院日,两组评分都呈现出总体下降的趋势。POD 2天没有评估疼痛评分。与此相反的是,Clark等人发现,术后初期的疼痛评分平均峰值下降,且有统计学意义(POD0:4.6±3.6 vs 6.5±3.5,P=0.004;POD1:5.2±3.5 vs 7.3±2.3,P=0.002;POD2:4.1±3.5 vs 6.6±2.8,P=0.002),与ERAS路径患者的疼痛评分总体下降趋势一致[38]。
接受游离皮瓣重建的HNC患者的术后疼痛管理是一项艰巨的任务。与其他癌症类型相比,HNC患者报告最多的症状就是疼痛[39]。患者进行头颈部的手术解剖部位不同,相关的疼痛症状也不同,游离皮瓣供体部位的疼痛可能最为剧烈[40-42]。此外,以局部和区域阻滞形式进行的额外镇痛干预往往不可用。本综述中纳入的6项研究支持Wick等人的大型系统综述的结果,肯定了MMA在ERAS路径中的安全性和有效性。为了实现最佳的疼痛管理,在整个围手术期继续使用MMA十分重要[24]。与Vu等人的研究结果相比,Eggerstedt等人、Jandali等人和Hinther等人的研究结果突出了连续MMA的重要性[33-36]。尽管他们使用了少量阿片类药物的镇痛方法,但Jandali等人和Kiong等人均报告称与对照组相比,ERAS组LOS(天数)有统计学意义上的减少[35,37]。在本综述中,没有研究发现两个组之间的ICU LOS有差异。对于包括非甾体抗炎药(nonsteroidal anti-inflammatory drugs,NSAIDs)的MMA方案,理论上存在着术后出血风险增加的可能性。一项对27项随机临床试验的系统回顾未能发现服用酮咯酸氨丁三醇的患者队列与对照组之间存在术后出血方面的差异[24]。在报告术后血肿发生率的6项研究中,有3项研究未发现ERAS组和对照组之间存在统计学上的显著差异。
疼痛是一种主观体验,受多种因素影响,难以衡量,临床上并不能通过直接测量确定疼痛存在统计学和临床意义上的缓解,也不能从一个结果中推断出另一个结果[43]。该领域的文献建议使用两种独立的疼痛评估方法,时间跨度至少为4天,以此得到令人满意的评估结果[30]。尽管已有多种疼痛评估工具,但疼痛结果的获取通常以患者的主观报告形式进行。本综述中的所有研究都是这种情况。大多数研究发现,在术后初期,疼痛程度有统计学意义上的减轻。此外,与对照组相比,ERAS组在整个过程中的平均得分较低,可见疼痛评分的整体下降趋势。限制疼痛评分在统计学上显著下降的因素可能是研究设计,而不是每个组的患者数量[43]。获得疼痛评分的频率、采用的疼痛量表以及用于评估总体趋势的指标可能需要修改[43]。Younger等人主张使用影响大小、特定的指标(如疼痛缓解的百分比)和表明有临床意义的变化的分界线[43]。疼痛评估领域的主要研究将疼痛减少30%视作有临床意义[44]。应用在本综述纳入的研究时,30%的减少相当于NRS 0~10中下降了2个数字[43,44]。
术后早期下床活动是HNC领域ERAS指南中的一个主要内容[3]。Twomey等人报告,在接受游离皮瓣重建的HNC ERAS组中,主要并发症较少,住院时间较短[45]。在一篇系统性综述中,Khan等人证明了遵循ERAS治疗路径的患者会取得更好的疼痛管理结果[19]。此外,其他外科领域的研究证明,有规划的疼痛管理方案对早期下床活动有利[46]。Clark等人在综述中表示,ERAS组的早期下床活动时间较早,平均时间(SD)为55.6(43.9)小时,而对照组则为93.4(63.9)小时(P=0.003)[38]。同样,Hinther等人和Jandali等人分别观察到ERAS患者术后活动时间的提前,且有临床意义[1.7(2.96)天 vs 2.5(2.12)天;P<0.001]和[1.4(1.3)天 vs 2.0(1.6)天;P=0.006] [35,36]。患者的早期活动时间受MMA控制疼痛的效果影响。
许多研究还报告了ERAS患者队列在术后和出院时减少了阿片类药物的使用,体现在阿片类药物开具处方减少。在其他外科领域发表的文章中,也发现了阿片类药物的消耗减少,这表明了患者的疼痛程度有所降低,但在ERAS和对照组之间的差异并不明显,没有统计学意义[47]。
围手术期和长期使用阿片类药物
阿片类药物是多家机构疼痛治疗方案的基石。麻醉性镇痛药可以有效地解决疼痛问题,但可能有严重的不良反应,包括呼吸抑制、恶心和呕吐、活动能力异常以及长期依赖的风险。据估计,多达80%的HNC患者都经历过疼痛,需要使用处方阿片类药物治疗[48]。但患者对基于阿片类药物的疼痛治疗的满意度很低,70%~85%的患者报告称疼痛控制效果不佳[25]。此外,手术类型可能与术后长期阿片类药物的消耗没有必然联系[29]。虽然导致需要长期使用阿片类药物的因素很多,但专注于HNC的研究已经确定了一些高危因素,包括术前有阿片类药物使用史、抽烟、种族、辅助治疗和晚期病理T阶段等[23,37]。
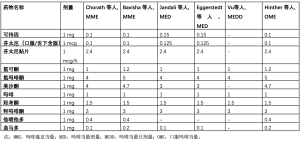
由于剂量转换方案不止一种,提供围手术期疼痛和阿片类药物使用的概述极富挑战性。仅此一点就可以说明,迄今为止,在关于HNC领域ERAS临床结果的系统性综述中,缺乏对阿片类药物使用结果的正式评估[9]。等效镇痛的概念可以定量地表示为两种阿片类药物为达到相当的镇痛效果所需的剂量[49]。将阿片类药物换算成基准指标,有助于医疗服务提供者比较多种药物的效力,并提供足够的镇痛效果[50]。等效镇痛可以有效预防意外过量,并最大限度地降低处方阿片类药物滥用的可能性[51]。换算计算器不是将一种药物的剂量转换为另一种药物的剂量,相反,当量系数允许操作者确定与其他各种含阿片类药物剂量相当的吗啡剂量,以反映药物的相对效力[50]。如此转换产生的数值被称为吗啡毫克当量(MME)。确定MME的计算方法通常需要考虑药物剂量、给药时间以及每种药物的特定转换系数。MME以标准化的方式反映患者消耗的阿片类药物总量,便于在发表的文献中对结果进行比较。吗啡当量剂量(MED)指患者在24小时内消耗的所有含有阿片剂的药物的总和。另一个参考指标是吗啡当量日剂量(MEDD)。MEDD被用作引起不良反应(包括过量)的潜在药物剂量相关风险的指标[52]。MEDD是以阈值的形式表示的,当阿片类药物达到一定限度时,患者的风险增加。最后,口服吗啡当量(OME)与MME类似,它是一种工具,由通过已发表的文章整理、综合而成的换算系数组成,可以促进阿片类药物使用研究结果的交流和比较[53]。根据手边的文献,MME、MED、MEDD和OME可以互换使用。要特别注意作者给出的定义和计算方法,这一点是解释所述结果的首要条件。本综述纳入的文章中使用的阿片类药物当量系数见表4。
Full table
3项研究发现ERAS患者在术后初期的阿片类药物消耗量减少[34,35,37]。Eggerstedt等人报道术后72小时内,MMA组的MED为10.0 MME(IQR:2.7~23.1),而对照组为89.6 MME(IQR:60~104.5)(P<0.001)[34]。Jandali等人发现,与对照组(82.7±116.1 mg;P<0.001)相比,ERAS组中的患者在术后72小时的平均MED(17.5±46.0 mg)明显降低表4 阿片类药物当量系数报告方案[35]。在同一时间段内,Kiong等人发现ERAS组的MME需求减少(138.8±181.5 vs 207.9±205.5;P<0.001),此外,术后PCA的使用需求也显著减少(31.0% vs 74.5%;P<0.001)[37]。为了便于比较,可以将Kiong等人报告的MME总值除以3来估计24小时内消耗的平均MED[37]。上述文章扩大了早期术后的概念,报告了出院时的阿片类药物使用情况。Eggerstedt等人发现MMA组出院时处方的MED中位数为0(IQR:0~18.8),而对照组为300.0(IQR:262.5~412.5)(P<0.001)[34]。
虽然其余3项研究报道了类似的趋势,但其研究设计是在一个较长的时间范围内记录术后阿片类药物的使用情况。Clark等人发现,与非ERAS组相比,ERAS组患者在POD 0~5天内的阿片类镇痛药物消耗量明显减少[38]。在术后总天数和每一天的测算中,平均MME消耗量的减少幅度都很显著(POD 0,校正后P=0.010;POD 1~5天,校正后P=0.000)。有趣的是,无论患者是否存在阿片类药物使用史,住院期间的阿片类药物消耗量都明显减少,并且没有影响疼痛管理方案。Hinther等人还对术后的时间窗进行了扩展性研究,观察到在POD 0~14天的整个过程中,MMA和低疼痛评分之间存在关联[36]。MMA组的平均每日阿片类药物消耗量为29.7 mg(SD 5.0),而对照组为43.3 mg(SD 18.8)(P=0.04 Wilcoxon)。在术后4天内,对照组的每日OME消耗量略低。术后4天后,对照组的OME消耗量要高得多。在住院期间,阿片类药物消耗的总体趋势为增加,尤其是在对照组。Vu等人量化了MEDD在两种环境下的阿片类药物使用量,即手术期间和在PACU时[33]。在两种环境综合考虑的情况下,与对照组患者相比,治疗组患者接受超过66 MEDD的阿片类药物的可能性降低了79%(OR:0.21;95% CI:0.12~0.36)。他们认为,术中及PACU期间给予一定量的阿片类药物即可产生适度的镇痛治疗效果,其原因为术前给予了超前镇痛。他们观察了在两种环境中实现MEDD临床意义上的减少的患者的百分比,然后进行了归纳总结。总体而言,在治疗组141例和对照组181例患者中,分别有92例(65.2%)和54例(29.8%)患者实现了临床意义上的MEDD减少,组间差异为35.4%(95%CI:24.6~45.0%)。在手术期间、PACU和综合考虑两种环境的情况下,治疗组实现了更高比例的临床意义上的MEDD减少。
Kiong等人指出,ERAS组中在出院时开具强阿片类镇痛药物的患者较少(64.5% vs 81.5%;P<0.001)[37]。该研究根据世界卫生组织的止痛阶梯和美国药物管理局的规定,将阿片类镇痛药物分为强效或弱效[37]。Jandali等人的研究表明,与对照组相比,ERAS组出院时使用麻醉药物的患者比例明显较低(21.7% vs 90.3%;P<0.001)[35]。在本综述纳入的研究中,这一比例最低。ERAS的效果可以持续较长一段时间。Jandali等人报告称,在术后30天内需要重新开具麻醉药物处方的患者较少(6.5% vs 36.6%;P<0.001)[35]。
所有研究都报告了术后阿片类药物的消耗剂量,对术后24小时至14天内使用的阿片类药物剂量进行了量化。在6项研究中,阿片类药物剂量的单位并不统一,分别用了OME、MED、MEDD和MME。与非ERAS组相比,所有ERAS组的术后阿片类药物使用量都有所减少。术前阿片类药物使用史是导致术后长期使用阿片类药物的一个已知危险因素[23]。本综述纳入的研究中,没有研究探讨患者术前使用阿片类药物的原因。一项研究确定了导致持续使用阿片类药物风险增加的因素,包括术前使用阿片类镇痛药物、既往放疗史、非裔美国人和ICU住院史[37]。虽然过去的研究确定了MMA能够减少HNC患者的阿片类药物用量,但受益的是接受ERAS部分方案的患者,而不是完整方案的患者[5,27]。
在现有研究中,对HNC领域ERAS患者阿片类镇痛药物用量的统计主要聚焦在术后即刻(72小时)和出院后1个月急性期的时间范围内。长期滥用阿片类药物指的是患者应用麻醉类药物时间长达90天以上,这项内容的具体情况目前在HNC领域ERAS患者人群中尚待进一步研究[23]。Hinther等人回顾性地量化了212例接受游离皮瓣重建的原发性HNC患者在3个月和12个月的阿片类药物使用情况,发现分别有136例(64%)和116例(55%)患者需要继续使用阿片类药物[36]。这些患者没有接受ERAS方案的全部内容,而只是接触了MMA部分。拥有完善的ERAS项目和良好的依从性的机构目前可能有能力研究其对疼痛和阿片类药物使用的长期影响。例如,Kiong等人对时间跨度为数月的传统匹配性队列研究上进行了改进,开展了时间跨度为2年,共纳入400例患者的病例匹配性队列研究[37]。
本综述纳入的研究的共同局限性包括,研究仅涉及了小范围患者人群,且试验设计为回顾性、观察性、开放性研究。考虑到科室资源、患者的教育水平和健康知识、协议遵守和人员培训以及医院的情况,ERAS在机构层面的实施不可避免地有所不同。根据不同地区的临床情况,不同的研究会根据阿片类药物的分配情况,使用不同类型的阿片类药物进行替代治疗。这种情况属于额外层面的、复杂的影响因素,这也强调了研究团队对研究设计进行仔细规划的必要性。在加州,对长期滥用阿片类药物患者进行前瞻性量化研究需要得到患者的知情同意,同时需要与管制类药物使用及审查评估系统(Controlled Substance Utilization and Review Evaluation System,CURES)合作。在量化术后阿片类药物的应用情况时,一个重要的局限性是缺乏队列匹配。例如,Jandali等人指出,对照组中明显有更多的患者在术前使用麻醉药物[35]。这可能是一个混杂因素,可能是导致与ERAS组相比,对照组在出院时麻醉药物处方开具增加的原因。对围手术期阿片类药物的使用进行正式分析具有挑战性。即使在本综述纳入的6篇文章中,也有4种不同的报告方案,即MME、OME、MED和MEDD。此外,作者可能会交替使用这些术语,尽管有时是错误的。采用一套可靠的等值系数将极大地促进ERAS对阿片类药物使用效果的评估。从理论上来说,72小时内的平均总MME可以除以3,以近似于3天内的平均MED。使用OME和MEDD量化阿片类药物使用的研究很难被纳入正式的评估。具体来说,与美国疾病控制中心(Centers for Disease Control,CDC)规定的MME比率相比,文献对OME当量比率的建议在氢可酮和美沙酮这两种药物之间有所不同[54]。如前所述,MEDD也使用一套等效系数来比较不同阿片类药物的效力。MEDD的一个具体作用是设定一个阈值,阻止进一步开具阿片类药物处方。由于这些阈值在不同的州和机构之间可能存在差异,MME将是一种更可靠的量化方法,方便进行数据比较。在未来,MME能带来正式评估和最终基于证据的HNC具体数据,从而为这一特定人群制定指南。进一步的研究将有助于识别和适当分流具有阿片类药物长期使用倾向的患者,安全地管理MMA,并监测疼痛情况,在有必要时适当地使用阿片类药物。
总结
ERAS医疗路径提供了基于循证医学的医疗建议,从而通过围手术期医疗经验为患者进行治疗。综述的文献强调了ERAS治疗策略中的多模式镇痛对减少围手术期疼痛和阿片类药物使用的重要作用。我们认为,对接受微血管游离皮瓣重建术的HNC患者如何采用ERAS路径,仍需要进一步研究,以便根据HNC的具体数据提出指导性建议。当分别使用数字评定量表(0~10)和MME换算方案对疼痛结果和阿片类药物使用情况进行测算时,可以对围手术期疼痛研究和阿片类药物使用情况的研究进行有效的比较。我们对当前文献进行了归纳总结,其结论为肿瘤切除和游离组织重建手术后的HNC患者使用MMA方案提供了理论依据。研究表明,使用MMA既能降低术后自我报告的疼痛评分,又能减少住院期间和出院后阿片类药物的应用剂量。但仍有一些问题值得进一步的研究及探索,从而优化在HNC患者人群中实施的MMA的具体方案。在未来的研究中,对疼痛和阿片类药物应用策略的标准化评估可以促进正式评估的发展,从而为HNC领域ERAS指南的制定奠定基础。
Acknowledgments
Funding: None.
Footnote
Reporting Checklist: The authors have completed the Narrative Review reporting checklist. Available at https://joma.amegroups.com/article/view/10.21037/joma-22-4/rc
Conflicts of Interest: All authors have completed the ICMJE uniform disclosure form (available at https://joma.amegroups.com/article/view/10.21037/joma-22-4/coif). The authors have no conflicts of interest to declare.
Ethical Statement: The authors are accountable for all aspects of the work in ensuring that questions related to the accuracy or integrity of any part of the work are appropriately investigated and resolved.
Open Access Statement: This is an Open Access article distributed in accordance with the Creative Commons Attribution-NonCommercial-NoDerivs 4.0 International License (CC BY-NC-ND 4.0), which permits the non-commercial replication and distribution of the article with the strict proviso that no changes or edits are made and the original work is properly cited (including links to both the formal publication through the relevant DOI and the license). See: https://creativecommons.org/licenses/by-nc-nd/4.0/.
References
- Ljungqvist O, Scott M, Fearon KC. Enhanced Recovery After Surgery: A Review. JAMA Surg 2017;152:292-8. [Crossref] [PubMed]
- Kehlet H. Multimodal approach to control postoperative pathophysiology and rehabilitation. Br J Anaesth 1997;78:606-17. [Crossref] [PubMed]
- Dort JC, Farwell DG, Findlay M, et al. Optimal Perioperative Care in Major Head and Neck Cancer Surgery With Free Flap Reconstruction: A Consensus Review and Recommendations From the Enhanced Recovery After Surgery Society. JAMA Otolaryngol Head Neck Surg 2017;143:292-303. [Crossref] [PubMed]
- Joshi GP, Kehlet H. Enhanced Recovery Pathways: Looking Into the Future. Anesth Analg 2019;128:5-7. [Crossref] [PubMed]
- Low GMI, Kiong KL, Amaku R, et al. Feasibility of an Enhanced Recovery After Surgery (ERAS) pathway for major head and neck oncologic surgery. Am J Otolaryngol 2020;41:102679. [Crossref] [PubMed]
- Bertelsen C, Hur K, Nurimba M, et al. Enhanced Recovery After Surgery-Based Perioperative Protocol for Head and Neck Free Flap Reconstruction. OTO Open 2020;4:2473974X20931037.
- Gemma M, Toma S, Lira Luce F, et al. Enhanced recovery program (ERP) in major laryngeal surgery: building a protocol and testing its feasibility. Acta Otorhinolaryngol Ital 2017;37:475-8. [Crossref] [PubMed]
- Bianchini C, Pelucchi S, Pastore A, et al. Enhanced recovery after surgery (ERAS) strategies: possible advantages also for head and neck surgery patients? Eur Arch Otorhinolaryngol 2014;271:439-43. [Crossref] [PubMed]
- Chorath K, Go B, Shinn JR, et al. Enhanced recovery after surgery for head and neck free flap reconstruction: A systematic review and meta-analysis. Oral Oncol 2021;113:105117. [Crossref] [PubMed]
- Gao LL, Basta M, Kanchwala SK, et al. Cost-effectiveness of microsurgical reconstruction for head and neck defects after oncologic resection. Head Neck 2017;39:541-7. [Crossref] [PubMed]
- Lewis CM, Aloia TA, Shi W, et al. Development and Feasibility of a Specialty-Specific National Surgical Quality Improvement Program (NSQIP): The Head and Neck-Reconstructive Surgery NSQIP. JAMA Otolaryngol Head Neck Surg 2016;142:321-7. [Crossref] [PubMed]
- Suh JD, Sercarz JA, Abemayor E, et al. Analysis of outcome and complications in 400 cases of microvascular head and neck reconstruction. Arch Otolaryngol Head Neck Surg 2004;130:962-6. [Crossref] [PubMed]
- Kearns M, Ermogenous P, Myers S, et al. Osteocutaneous flaps for head and neck reconstruction: A focused evaluation of donor site morbidity and patient reported outcome measures in different reconstruction options. Arch Plast Surg 2018;45:495-503. [Crossref] [PubMed]
- Kleppe KL, Greenberg JA. Enhanced Recovery After Surgery Protocols: Rationale and Components. Surg Clin North Am 2018;98:499-509. [Crossref] [PubMed]
- Rice D, Rodriguez-Restrepo A, Mena G, et al. Matched Pairs Comparison of an Enhanced Recovery Pathway Versus Conventional Management on Opioid Exposure and Pain Control in Patients Undergoing Lung Surgery. Ann Surg 2021;274:1099-106. [Crossref] [PubMed]
- Melloul E, Lassen K, Roulin D, et al. Guidelines for Perioperative Care for Pancreatoduodenectomy: Enhanced Recovery After Surgery (ERAS) Recommendations 2019. World J Surg 2020;44:2056-84. [Crossref] [PubMed]
- Gustafsson UO, Scott MJ, Hubner M, et al. Guidelines for Perioperative Care in Elective Colorectal Surgery: Enhanced Recovery After Surgery (ERAS®) Society Recommendations: 2018. World J Surg 2019;43:659-95. [Crossref] [PubMed]
- Tan YY, Liaw F, Warner R, et al. Enhanced Recovery Pathways for Flap-Based Reconstruction: Systematic Review and Meta-Analysis. Aesthetic Plast Surg 2021;45:2096-115. [Crossref] [PubMed]
- Khan S, Wilson T, Ahmed J, et al. Quality of life and patient satisfaction with enhanced recovery protocols. Colorectal Dis 2010;12:1175-82. [Crossref] [PubMed]
- van den Beuken-van Everdingen MH, de Rijke JM, Kessels AG, et al. Prevalence of pain in patients with cancer: a systematic review of the past 40 years. Ann Oncol 2007;18:1437-49. [Crossref] [PubMed]
- Cramer JD, Johnson JT, Nilsen ML. Pain in Head and Neck Cancer Survivors: Prevalence, Predictors, and Quality-of-Life Impact. Otolaryngol Head Neck Surg 2018;159:853-8. [Crossref] [PubMed]
- Pang J, Tringale KR, Tapia VJ, et al. Chronic Opioid Use Following Surgery for Oral Cavity Cancer. JAMA Otolaryngol Head Neck Surg 2017;143:1187-94. [Crossref] [PubMed]
- Hinther A, Abdel-Rahman O, Cheung WY, et al. Chronic Postoperative Opioid Use: A Systematic Review. World J Surg 2019;43:2164-74. [Crossref] [PubMed]
- Wick EC, Grant MC, Wu CL. Postoperative Multimodal Analgesia Pain Management With Nonopioid Analgesics and Techniques: A Review. JAMA Surg 2017;152:691-7. [Crossref] [PubMed]
- Hinther A, Nakoneshny SC, Chandarana SP, et al. Efficacy of postoperative pain management in head and neck cancer patients. J Otolaryngol Head Neck Surg 2018;47:29. [Crossref] [PubMed]
- Hinther A, Rasool A, Nakoneshny SC, et al. Chronic opioid use following surgery for head and neck cancer patients undergoing free flap reconstruction. J Otolaryngol Head Neck Surg 2021;50:28. [Crossref] [PubMed]
- Du E, Farzal Z, Stephenson E, et al. Multimodal Analgesia Protocol after Head and Neck Surgery: Effect on Opioid Use and Pain Control. Otolaryngol Head Neck Surg 2019;161:424-30. [Crossref] [PubMed]
- Lee TS, Wang LL, Yi DI, et al. Opioid sparing multimodal analgesia treats pain after head and neck microvascular reconstruction. Laryngoscope 2020;130:1686-91. [Crossref] [PubMed]
- Brummett CM, Waljee JF, Goesling J, et al. New Persistent Opioid Use After Minor and Major Surgical Procedures in US Adults. JAMA Surg 2017;152:e170504. [Crossref] [PubMed]
- Jensen MP, McFarland CA. Increasing the reliability and validity of pain intensity measurement in chronic pain patients. Pain 1993;55:195-203. [Crossref] [PubMed]
- Hawker GA, Mian S, Kendzerska T, et al. Measures of adult pain: Visual Analog Scale for Pain (VAS Pain), Numeric Rating Scale for Pain (NRS Pain), McGill Pain Questionnaire (MPQ), Short-Form McGill Pain Questionnaire (SF-MPQ), Chronic Pain Grade Scale (CPGS), Short Form-36 Bodily Pain Scale (SF-36 BPS), and Measure of Intermittent and Constant Osteoarthritis Pain (ICOAP). Arthritis Care Res (Hoboken) 2011;63:S240-52. [Crossref] [PubMed]
- Buckenmaier CC 3rd, Galloway KT, Polomano RC, et al. Preliminary validation of the Defense and Veterans Pain Rating Scale (DVPRS) in a military population. Pain Med 2013;14:110-23. [Crossref] [PubMed]
- Vu CN, Lewis CM, Bailard NS, et al. Association Between Multimodal Analgesia Administration and Perioperative Opioid Requirements in Patients Undergoing Head and Neck Surgery With Free Flap Reconstruction. JAMA Otolaryngol Head Neck Surg 2020;146:708-13. [Crossref] [PubMed]
- Eggerstedt M, Stenson KM, Ramirez EA, et al. Association of Perioperative Opioid-Sparing Multimodal Analgesia With Narcotic Use and Pain Control After Head and Neck Free Flap Reconstruction. JAMA Facial Plast Surg 2019;21:446-51. [Crossref] [PubMed]
- Jandali DB, Vaughan D, Eggerstedt M, et al. Enhanced recovery after surgery in head and neck surgery: Reduced opioid use and length of stay. Laryngoscope 2020;130:1227-32. [Crossref] [PubMed]
- Hinther A, Nakoneshny SC, Chandarana SP, et al. Efficacy of Multimodal Analgesia for Postoperative Pain Management in Head and Neck Cancer Patients. Cancers (Basel) 2021;13:1266. [Crossref] [PubMed]
- Kiong KL, Vu CN, Yao CMKL, et al. Enhanced Recovery After Surgery (ERAS) in Head and Neck Oncologic Surgery: A Case-Matched Analysis of Perioperative and Pain Outcomes. Ann Surg Oncol 2021;28:867-76. [Crossref] [PubMed]
- Clark BS, Swanson M, Widjaja W, et al. ERAS for Head and Neck Tissue Transfer Reduces Opioid Usage, Peak Pain Scores, and Blood Utilization. Laryngoscope 2021;131:E792-9. [Crossref] [PubMed]
- Grond S, Zech D, Lynch J, et al. Validation of World Health Organization guidelines for pain relief in head and neck cancer. A prospective study. Ann Otol Rhinol Laryngol 1993;102:342-8. [Crossref] [PubMed]
- Sullivan MD, Bauer AM, Fulton-Kehoe D, et al. Trends in Opioid Dosing Among Washington State Medicaid Patients Before and After Opioid Dosing Guideline Implementation. J Pain 2016;17:561-8. [Crossref] [PubMed]
- Gil Z, Smith DB, Marouani N, et al. Treatment of pain after head and neck surgeries: control of acute pain after head and neck oncological surgeries. Otolaryngol Head Neck Surg 2006;135:182-8. [Crossref] [PubMed]
- Chiu TW, Leung CC, Lau EY, et al. Analgesic effects of preoperative gabapentin after tongue reconstruction with the anterolateral thigh flap. Hong Kong Med J 2012;18:30-4. [PubMed]
- Younger J, McCue R, Mackey S. Pain outcomes: a brief review of instruments and techniques. Curr Pain Headache Rep 2009;13:39-43. [Crossref] [PubMed]
- Farrar JT, Young JP Jr, LaMoreaux L, et al. Clinical importance of changes in chronic pain intensity measured on an 11-point numerical pain rating scale. Pain 2001;94:149-58. [Crossref] [PubMed]
- Twomey R, Matthews TW, Nakoneshny S, et al. Impact of Early Mobilization on Recovery after Major Head and Neck Surgery with Free Flap Reconstruction. Cancers (Basel) 2021;13:2852. [Crossref] [PubMed]
- Nachiyunde B, Lam L. The efficacy of different modes of analgesia in postoperative pain management and early mobilization in postoperative cardiac surgical patients: A systematic review. Ann Card Anaesth 2018;21:363-70. [Crossref] [PubMed]
- Dietz N, Sharma M, Adams S, et al. Enhanced Recovery After Surgery (ERAS) for Spine Surgery: A Systematic Review. World Neurosurg 2019;130:415-26. [Crossref] [PubMed]
- Schaller AKCS, Peterson A, Bäckryd E. Pain management in patients undergoing radiation therapy for head and neck cancer - a descriptive study. Scand J Pain 2021;21:256-65. [Crossref] [PubMed]
- Bhatnagar M, Pruskowski J. Opioid Equivalency. In: StatPearls. 2021, StatPearls Publishing Copyright © 2021, StatPearls Publishing LLC.: Treasure Island (FL).
- Treillet E, Laurent S, Hadjiat Y. Practical management of opioid rotation and equianalgesia. J Pain Res 2018;11:2587-601. [Crossref] [PubMed]
- Dowell D, Haegerich TM, Chou R. CDC Guideline for Prescribing Opioids for Chronic Pain--United States, 2016. JAMA 2016;315:1624-45. [Crossref] [PubMed]
- Clinical Review Update: Morphine Equivalent Daily Dose. February 28, 2019.
- Nielsen S, Degenhardt L, Hoban B, et al. A synthesis of oral morphine equivalents (OME) for opioid utilisation studies. Pharmacoepidemiol Drug Saf 2016;25:733-7. [Crossref] [PubMed]
- (CDC), U.D.o.H.a.H.S.-C.f.D.C.a.P. Calculating Total Daily Dose of Opioids for Safer Dosage. [cited 2021 December 5]. Available online: https://www.cdc.gov/drugoverdose/pdf/calculating_total_daily_dose-a.pdf

夏明
Journal of Oral and Maxillofacial Anesthesia (JOMA)执行主编。上海交通大学医学院附属第九人民医院麻醉科副主任医师,副教授,硕士研究生导师;麻醉学博士,博士后。现担任中华口腔医学会口腔麻醉学专业委员会全国常务委员、上海市疼痛科临床质量控制中心专家委员会委员、中华口腔医学会镇静镇痛分会全国委员等学术职务。(更新时间:2022/8/4)
(本译文仅供学术交流,实际内容请以英文原文为准。)
Cite this article as: Castellanos CX, Ulloa R, Kim C, Tang L, Swanson M, Kokot N. Enhanced recovery after surgery: a narrative review on perioperative pain levels and opiate use following free flap reconstruction in patients with head and neck cancer. J Oral Maxillofac Anesth 2022;1:14.




